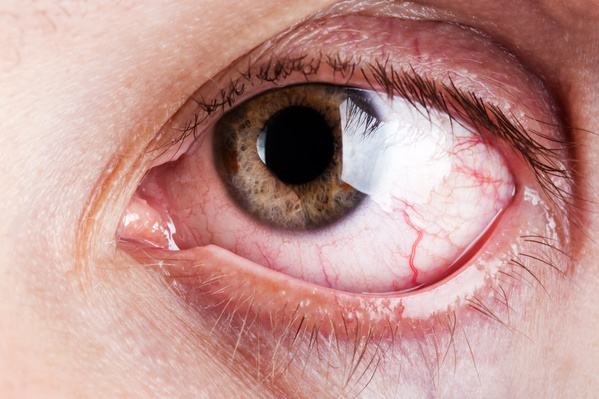
Novaliq, azienda biofarmaceutica che si dedica allo sviluppo di terapie oculari della massima qualità basate sull’esclusiva tecnologia senz’acqua EyeSol, ha annunciato l’intenzione di depositare una richiesta di autorizzazione all’immissione in commercio nell’Unione europea per CyclASol (soluzione oftalmica a base di ciclosporina), un prodotto antinfiammatorio innovativo per il trattamento della sindrome dell’occhio secco (DED). Il Comitato per i medicinali per uso umano (CHMP) dell’Agenzia europea per i medicinali (EMA) ha stabilito che il CyclASol è idoneo alla revisione in una procedura centralizzata per ricevere un’autorizzazione all’immissione in commercio nello Spazio economico europeo (SEE). Nel dicembre 2022, l’EMA ha dichiarato nella sua risposta che, sulla base della documentazione fornita da Novaliq, una presentazione è nell’interesse dei pazienti a livello comunitario ai sensi dell’Articolo 3(2)b – Interesse dei pazienti del Regolamento (CE) n. 726/2004. Di conseguenza, Novaliq ha presentato una lettera di intenti all’EMA per il deposito di una richiesta di autorizzazione all’immissione in commercio nel luglio 2023.
Cerca articoli
Articoli recenti
- I PFAS modificano i livelli di calcio nel corpo
- Proteintech, con 3D Epitope Mapping di nuova generazione si accelera la ricerca nelle scienze della vita
- Disturbi alimentari, al Bambin Gesù +60% di nuovi casi dal 2019
- I disegni dei pazienti del Bambin Gesù per il Papa
- “Dopo il glaucoma mi chiamavano Polifemo”. Cosa ha da dire la storia di Renato a 1 milioni di Italiani